
Vörukynning
| Kalsíumflúoríð Grunnupplýsingar |
| Efnafræðilegir eiginleikar kristalbygging Notar framleiðsluaðferð |
| Vöruheiti: | Kalsíumflúoríð |
| Samheiti: | Kalsíumflúoríð; Kalsíumflúoríð, 99,9% snefilmálma grundvöllur; Kalsíumflúoríð, 99,95% snefilmálma grundvöllur; Kalsíumflúoríð, vatnsfrítt, fyllt undir argon, 99,99% snefilmálma grundvöllur; Kalsíumflúoríð í Kína) ANTI-CNTEROT8; framleitt í kanínum;CAF1-líkt próteini;CALIFp |
| CAS: | 7789-75-5 |
| MF: | CaF2 |
| MW: | 78.07 |
| EINECS: | 232-188-7 |
| Vöruflokkar: | Ólífræn efni; málmhalíð |
| Mol skrá: | 7789-75-5.mól |
 |
|
| Kalsíumflúoríð Efnafræðilegir eiginleikar |
| Bræðslumark | 1402 gráður |
| Suðumark | 2500 gráður (lit.) |
| þéttleika | 3,18 g/ml við 25 gráður (lit.) |
| brotstuðull | 1.434 |
| Fp | 2500 gráður |
| geymsluhitastig. | -20 gráðu |
| leysni | Lítið leysanlegt í sýru; óleysanlegt í asetoni. |
| formi | stöng |
| lit | hvítur |
| Eðlisþyngd | 3.18 |
| Vatnsleysni | 0.015 g. á 100g H20 við stofuhita.(Óleysanlegt) |
| Viðkvæm | Vökvasöfnun |
| Merck | 14,1667 |
| Leysni vara stöðug (Ksp) | pKsp: 8,28 |
| Útsetningarmörk | ACGIH: TWA 2,5 mg/m3 NIOSH: IDLH 250 mg/m3; TWA 2,5 mg/m3 |
| Rafstuðull | 2,5 (umhverfi) |
| Stöðugleiki: | Stöðugt. Kalsíumflúoríð er óvirkt fyrir lífrænum efnum og mörgum sýrum, þar á meðal HF. Það leysist hægt upp í saltpéturssýru. |
| InChIKey | WUKWITHWXAAZEY-UHFFFAOYSA-L |
| Tilvísun í CAS gagnagrunn | 7789-75-5(CAS DataBase Reference) |
| NIST efnafræði tilvísun | Kalsíumflúoríð(7789-75-5) |
| EPA efnisskrárkerfi | Kalsíumdíflúoríð (7789-75-5) |
| Öryggisupplýsingar |
| Hættukóðar | Xi,Xn |
| Áhættuyfirlýsingar | 36/37/38 |
| Öryggisyfirlýsingar | 26-37/39-36 |
| RIDADR | 3288 |
| WGK Þýskalandi | 1 |
| RTECS | EW1760000 |
| Hættuathugið | Ertandi |
| TSCA | Já |
| HS kóða | 28261900 |
| Gögn um hættuleg efni | 7789-75-5(Hættuleg efni) |
| Eiturhrif | LD50 ip í músum: 2638,27 mg/kg (Stratmann) |
| MSDS upplýsingar |
| Veitandi | Tungumál |
|---|---|
| Kalsíumflúoríð | ensku |
| Sigma Aldrich | ensku |
| ACROS | ensku |
| ALFA | ensku |
| Kalsíumflúoríð notkun og myndun |
| Efnafræðilegir eiginleikar | Kalsíumflúoríð er aðal innihaldsefnið í flúorspar eða flúorít, efnaformúlan er CaF2, það er litlaus kúbískur kristal eða hvítt duft. Hlutfallslegur eðlismassi er 3,18, bræðslumark er 1423 gráður, suðumark er um 2500 gráður. Leysni í vatni er í lágmarki, 100g vatn getur aðeins leyst upp 0,0016g við 18 gráður, það er óleysanlegt í asetoni, en leysanlegt í saltsýru, flúorsýru, brennisteinssýru, saltpéturssýru og ammóníumsaltlausn, og það getur ekki brugðist við þynntri sýru, en getur hvarfast við heita óblandaða brennisteinssýru og myndað flúorsýru, það getur myndað flókið þegar það leysist upp í ál- og járnsöltum (Fe3 +) lausn. Náttúrulegt kalsíumflúoríð er steinefni flúorít eða flússpat, sýnir oft gráa, gula, græna, fjólubláa og aðra liti, stundum er það litlaus, gagnsætt, glansandi gler, brothætt, og hlutfallslegur þéttleiki er 3,01 ~ 3,25, það hefur verulegt fyrirbæri flúrljómunar. Það er hægt að nota sem uppspretta flúors og efnið til að búa til flúorsýrukerfi, flúoríð; og það er einnig hægt að nota hvað varðar framleiðslu á gleri, enamel, gljáa. Flúorít er aðallega notað sem flæði í málmvinnslu, mjög hreint flúorspar er hægt að nota til að búa til sérstakar linsur. Vatn þegar það inniheldur (1~1,5) × 10-6 kalsíumflúoríð getur komið í veg fyrir tannvandamál. Að auki er hægt að nota það í bræðslu járns og stáls, efna, glers, keramikframleiðslu. Hægt er að nota hreina vöru sem hvata fyrir þurrkun, afvötnun. Með áhrifum leysanlegra kalsíumsölta (kalsíumkarbónat eða kalsíumhýdroxíðs) og natríumflúoríðs eða flúorsýra er hægt að fá ammóníumflúoríð, kalsíumflúoríð. |
| kristal uppbyggingu | Kalsíumflúoríð er jónandi kristal með flúoranjónum í einföldum teningaflokki og kalsíumkatjónir í helmingi teningsstaða byggingarinnar. Einnig er hægt að hugsa sér að kalsíumjónirnar séu á „stækkaðri“ fcc grind með flúorjónunum sem veldur því að grindarskil þeirra er 0.39 nm. Þessi framsetning er sýnd á neðri skýringarmyndinni. Einingaklefan hefur 4 Ca2+jónir og 8 F1-jónir.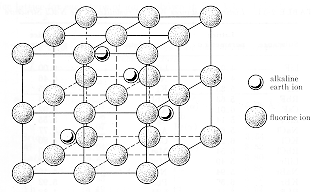 Efnið er gegnsætt á sýnilega litrófssvæðinu og sýnir rafrænt sjónaðsog í útfjólubláu og sjónrænu frásog grindar í innrauða. |
| Notar |
Iðnaður
Umsókn
Hlutverk/ávinningur
Efnaframleiðsla
Framleiðsla á flúorsýru og flúoríði
Hráefni/flúoruppspretta
Framleiðsla á flúorfínefnum og tilbúnu krýólíti
Hráefni/flúoruppspretta
Byggingarefni
Framleiðsla á gleri
Flæðiefni/stuðla að bráðnun hráefna
Framleiðsla á sementi
Mineralization efni
Framleiðsla á keramik gljáa
Flux og litarefni
Málmvinnsla
Járn- og stálbræðsla, járnblendiframleiðsla osfrv.
Flæðiefni/lækkar bræðslumark eldföstra efna
Lyf
Meðferð, stjórn, forvarnir og úrbætur á ofnæmisviðbrögðum
Stuðla að nýmyndun beina
Hitamyndakerfi, litrófsgreiningar, sjónaukar og excimer leysir
Framleiðsla á optískum íhlutum, svo sem gluggum og linsum
Hráefni/breitt svið ljósssendingatíðna; lágt brotstuðul; hár hitastöðugleiki
Aðrir
Framleiðsla suðuefna
Mikilvægir þættir í húðun á suðustöngum og suðudufti
Ofþornun og afvötnunarviðbrögð
Hvati/hraða hvarfferli
Framleiðsla á bremsuklæðningu
Aukefni/hjálpar til við að draga úr núningi af völdum mikils hita og núnings
|
| Framleiðsluaðferð | Flúorítútfellingarnar sem fundist hafa í Kína eru aðallega notaðar í námuna með því að nota neðanjarðar námuvinnsluaðferð, eða grunna námuvinnslu í opnum holum, og neðanjarðar djúpnámu, fyrir málmgrýti líkamans mest halla æð, framlengingin er einnig stór. Námuvinnsluaðferð er byggð á grunnu holu Rýrnunaraðferð byggð. Námuvinnsluferli sér "fosfatberg." Nýtingaraðferðir eru yfirleitt tvenns konar, önnur er óunnin málmgrýti sem getur orðið hæft málmgrýtiþykkni með því að meðhöndla valið, sú seinni er handvalið magurt málmgrýti og úrgangs. |
| Lýsing | Kalsíumflúoríð er litlaus kristallað eða hvítt, duftkennt efni. Mólþyngd{{0}}.08;Sérstakur þyngdarafl (H2O:1)=3.18 við 20 gráður ; Suðumark=2495 gráðu ; Frost-/bræðslumark=1423 gráðu . Hættuauðkenning (byggt á NFPA-704 M einkunnakerfi): Heilsa 2, Eldfimi 0, hvarfvirkni 0. Nánast óleysanlegt vatn. |
| Efnafræðilegir eiginleikar | Kalsíumflúoríð, CaF2, einnig þekkt sem flúorít og feldspat, er litlaus fast efni sem samanstendur af teningskristöllum. Það hefur lítið vatnsleysni, en er auðveldlega leysanlegt í ammoníumsaltlausnum. Kalsíumflúoríð er notað við myndun flúorsýru og í ætingargler. Kalsíumflúoríð er ekki rakafræðilegt og er tiltölulega óvirkt. Það hefur nægilega mikla viðnám gegn hitauppstreymi og vélrænum áföllum og það er auðvelt að búa til margs konar skynjara rúmfræði. Kalsíumflúoríð hefur mjög lágan gufuþrýsting, sem gerir það kleift að nota það í margs konar lofttæmisnotkun. Það er óleysanlegt í vatni og flestum lífrænum leysum, sem gerir kleift að koma geislavirkum sýnum í lausn í beina snertingu við kristalinn. Kalsíumflúoríð er gagnsætt efni sem notað er til að greina -geisla allt að nokkur hundruð keV og til að greina hlaðnar agnir. Vegna lágrar lotutölu er ljósbrot efnisins tiltölulega lítið sem takmarkar notkun þess í geislum við hærri orku. Hins vegar gerir lág atómatalan kalsíumflúoríð að kjörnu efni til að greina -agnir vegna lítillar bakdreifingar. |
| Eðliseiginleikar | Hvítur teningur kristal eða duft; brotstuðull 1.434; þéttleiki 3,18 g/cm3; hörku 4 Mohs; bráðnar við 1.418 gráður; gufar við 2.533 gráður; óleysanlegt í vatni (16 mg/L við 20 gráður); Ksp 3,9x10-11; örlítið leysanlegt í þynntri steinefnasýru; leysanlegt í óblandaðri sýru (með hvarfi). |
| Notar | Náttúrulegt CaF2 er helsta uppspretta vetnisflúoríðs, hráefna sem er notað til að framleiða fjölbreytt úrval af efnum. Flúor er losað úr steinefninu með verkun óblandaðri brennisteinssýru: CaF2 (fast)+H2SO4 (fljótandi)→CaSO4 (fast)+2HF (gas) CaF2 er notað sem optískur hluti vegna efnafræðilegs stöðugleika við slæmar aðstæður. Kalsíumflúoríð er almennt notað sem gluggaefni fyrir bæði innrauða og útfjólubláa bylgjulengd, þar sem það er gegnsætt á þessum svæðum (um 0.15 til 9 mm) og sýnir mjög lágan brotstuðul. Kalsíumflúoríð er vatnsóleysanleg kalsíumgjafi til notkunar í súrefnisnæmum forritum, svo sem málmframleiðslu. Í mjög lágum styrk (ppm) eru flúoríðsambönd notuð í heilsufarslegum tilgangi. Flúorsambönd hafa einnig verulega notkun í tilbúinni lífrænni efnafræði. Þeir eru einnig almennt notaðir til að blanda málm og fyrir sjónútfellingu. Það er einnig notað sem flæði til bræðslu og fljótandi vinnslu á járni, stáli og samsettum efnum þeirra. Verkun þess byggist á svipuðu bræðslumarki og járn, á getu þess til að leysa upp oxíð og á getu þess til að bleyta oxíð og málma. |
| Notar | Flúorspat er aðaluppspretta flúors og efnasambanda þess. Í járnmálmvinnslu er það notað sem flæði til að auka vökva gjallsins. Stáliðnaðurinn er stærsti neytandinn; efnaiðnaður, annað og gler og keramik, þriðja. Tilbúið flússpat er notað í ljóstækniiðnaðinum (sendur útfjólubláa geisla) og hreint kalsíumflúoríð er notað sem hvati í þurrkun og afvötnun. Notað til að flúorera drykkjarvatn. |
| Notar | Kalsíumflúoríð er viðskiptalega mikilvæg uppspretta fyrir flúorefnasambönd sem og vetnisflúoríð. Það er gegnsætt frá útfjólubláu til innrauðu svæði. Það er notað í litrófsgreiningu, hitamyndatökukerfum og excimer leysigeislum; það er einnig notað við framleiðslu á optískum íhlutum þar á meðal glugga, prisma og linsur. Að auki er það einnig notað í ál-málmvinnslu, bremsufóðaframleiðsluiðnaði og í tannglerung. |
| Skilgreining | Hreint náttúrulegt form kalsíumflúoríðs. |
| Framleiðsluaðferðir | Auglýsingavaran er fengin úr náttúrulegu steinefni flússpat, sem er hreinsað og duftformað. Einnig er hægt að fella það út með því að blanda lausn af natríumflúoríði við leysanlegt kalsíumsalti: Ca(NO3)2+ 2NaF → CaF2+ NaNO3 Að öðrum kosti er hægt að fá það með því að meðhöndla kalsíumkarbónat með flúorsýru:CaCO3+ 2HF → CaF2+ CO2 + H2O. |
| Skilgreining | Steinefnaform kalsíumflúoríðs (CaF2), notað til að búa til sumt sement og glergerðir. |
| Almenn lýsing | Lyktarlaust grátt duft eða korn. Sekkur í vatni. |
| Viðbragðsprófíll | Kalsíumflúoríð hefur veikburða oxandi eða afoxandi eiginleika. Enduroxunarviðbrögð geta samt komið fram. Meirihluti efnasambanda í þessum flokki eru lítillega leysanleg eða óleysanleg í vatni. Ef þær eru leysanlegar í vatni eru lausnirnar yfirleitt hvorki mjög súrar né mjög basískar. Þessi efnasambönd eru ekki hvarfgjörn fyrir vatni. |
| Hættan | Ertandi. |
| Heilsuhætta | Lítil bráð eituráhrif |
| Eldfimi og sprengihæfni | Ekki eldfimt |
| Iðnaðarnotkun | Einnig kallað flúorít, flúorspar er kristallað eða gríðarlegt kornótt steinefni í samsetningunni CaF2, notað sem flæði við framleiðslu á stáli, til að búa til flúorsýru, í ópallýsandi gler, í keramik glerung, til að slípa gervi krýólít, sem bindiefni fyrir gleraugu slípihjól og við framleiðslu á hvítu sementi. Það er betra flæði fyrir stál en kalksteinn, myndar fljótandi gjall og losar járnið við brennisteini og fosfór. Acid spar er einkunn sem notuð er til að búa til flúorsýru. Það er einnig notað til að búa til kælimiðla, plast og efni og til að draga úr áli. Optical flourspar er hæsta einkunn en er ekki algeng. Flúorkristallar fyrir sjónlinsur eru ræktaðir tilbúnar úr sýrustigs flússpat. Hreint kalsíumflúoríð, Ca2F6, er litlaus kristallað duft sem notað er til að æta gler, í glerung og til að draga úr núningi í vélalegum. Það er einnig notað fyrir keramikhluta sem eru þola flúorsýru og flestar aðrar sýrur. Kalsíumflúorít hefur sílikon í sameindinni og er kristallað duft sem notað er í glerung. Tæru rhombic flúoríð kristallarnir sem notaðir eru til að umbreyta raforku í ljós eru blý flúoríð, PbF2. |
| Öryggissnið | Miðlungs eitrað í kviðarholi. Vægt eitrað við inntöku. Vansköpunarvaldur í tilraunaskyni. Önnur tilraunaáhrif á æxlun. Stökkbreytingargögn tilkynnt. Sjá einnig FLÚORÍÐ OG KALSÍUMEFNI. Þegar það er hitað til niðurbrots gefur það frá sér eitraðar gufur af F-. |
| Mögulegt smit | Kalsíumflúoríð er notað til framleiðslu á flúorsýru; sem flæði í stálframleiðslu; í bræðslu; rafbogasuðu, gerð gler og keramik; og að flúoríða drykkjarvatni. |
| Skyndihjálp | Ef þetta efni kemst í augun skaltu fjarlægja allar augnlinsur í einu og skola strax í að minnsta kosti 15 mínútur, lyftu efri og neðri augnlokum af og til. Leitaðu tafarlaust til læknis. Ef þetta efni kemst í snertingu við húðina skaltu fjarlægja mengaðan fatnað og þvo hann strax með sápu og vatni. Leitaðu tafarlaust til læknis. Ef þessu efni hefur verið andað að sér, fjarlægðu úr útsetningu, byrjaðu að bjarga öndun (með því að nota alhliða varúðarráðstafanir, þar á meðal endurlífgunargrímu) ef öndun hefur stöðvast og endurlífgun ef hjartastarfsemi hefur stöðvast. Flutningur tafarlaust á sjúkrastofnun. Leitaðu til læknis þegar þetta efni hefur verið gleypt. Viðurkenndur sjúkraliði getur íhugað að gefa álhýdroxíðhlaup ef hann er með meðvitund. |
| geymsla | Litakóði-grænn: Nota má almenna geymslu. Geymið í vel lokuðum umbúðum á köldum, vel loftræstum stað fjarri sýrum og efnafræðilega virkum málmum (svo sem kalíum, natríum, magnesíum og sink) vegna þess að ætandi vetnisflúoríð myndast. |
| Sending | Kalsíumflúoríð fellur ekki sérstaklega undir DOT í frammistöðumiðuðum umbúðastöðlum. |
| Ósamrýmanleiki | Ryk getur myndað sprengifima blöndu með lofti. Hvarfast við vatn, rakt loft og gufu og losar eldfimt vetnisgas; og getur sjálfkviknað í lofti. Sterkt afoxunarefni; ósamrýmanleg oxunarefnum (klóröt, nítröt, peroxíð, permanganöt, perklóröt, klór, bróm, flúor osfrv.); snerting getur valdið eldi eða sprengingum. Geymið fjarri basískum efnum, sterkum basa, sterkum sýrum, oxósýrum, epoxíðum. Ósamrýmanlegt málmhalógenötum, silfurflúoríði og tetrahýdrófúrani |
| Kalsíumflúoríð undirbúningsvörur og hráefni |
| Hráefni | Hydrogen fluoride-->Calcium hydroxide-->CARBON MONOXIDE-->Quartz-->Calcium acetate-->kalsíum magnesíum fosfat (CMP) |
| Undirbúningsvörur | Hydrogen fluoride-->Boron trifluoride diethyl etherate-->Potassium Phosphate Monobasic-->Hexafluorosilicic acid-->Calcium cyanamide-->Sodium fluoride-->Trisodium hexafluoroaluminate-->Aluminum fluoride-->bastnasite-->Carbon tetrafluoride-->cryolite-->ZINC SILICOFLUORIDE-->MAGNESIUM HEXAFLUOROASETYLACETONATE DIHYDRATE |
maq per Qat: sink flúoríð, Kína sink flúor framleiðendur, birgjar, verksmiðju
chopmeH: Sirkonflúoríð
veb: Kalsíumflúoríð
Þér gæti einnig líkað
Hringdu í okkur


